类器官串联芯片培养系统—HUMIMIC
类器官串联芯片培养系统--- HUMIMIC
类器官技术平台是一种微流控微生理系统平台,能够维持和培养微缩的类器官,模拟其各自的全尺寸对应器官的生物学功能和生物的主要特征,如生物流体流动,机械和电耦合,生理组织与流体、组织与组织的比例。
TissUse的HUMIMIC®类器官串联芯片培养系统通过一个自动化设备来控制不同的芯片形式。比如HUMIMIC®Chip2芯片,能够在每个芯片的两个微流道连接的培养室中培养两个不同或者相同的器官。芯片上的微泵在每个微流道中产生生理脉动液体循环流动。培养室可以灵活地装载任何类型的器官,包括基于transwell的培养小室。芯片的底部是光学透明的玻璃,可以实现实时成像。
TissUse的HUMIMIC®类器官串联芯片培养系统是通过芯片完成微流体环境中的器官培养,可以维持更复杂的条件,包括物理因素,如温度(如37°C)、pH值、氧气和湿度的供应和控制;包括仿生机械学因素,例如:血液或尿液的流动,空气在肺中的循环,胆汁或胰液的流动,血液和淋巴管的剪切应力,骨骼和软骨的压力,皮肤的压力、肺或胃的外壁,肠的蠕动运动,肌肉收缩等等;包括括神经元和心脏组织的电信号,通过连接相关的小型化致动器和传感器具备了在体内模拟组织特异性机电-生化信号的必要功能,能够为肺、骨和软骨提供扩张和压缩力,以及用于电刺激和肌肉组织读出的微电极或刺激心肌细胞或神经元。
TissUse的HUMIMIC®类器官串联芯片培养系统包括控制单元和芯片,控制单元能够模拟人体内生理环境,包括温度、压力、真空度、微流道循环频率、时间等参数,芯片有不同的微流道设计,针对不同的器官可以单独设置提供相应的培养条件,提供精准的培养和分化环境。可提供不同类器官的串联共培养方案,避免单一类器官无法模拟人体复杂生理学条件下器官相互通讯交流的不足。通过类器官模拟人类器官组织的生理发育过程,应用于疾病模型、肿瘤发生、以及药物安全性、有效性、毒性、ADME等方面的评估,旨在减少和取代实验室动物测试,简化人体临床试验。
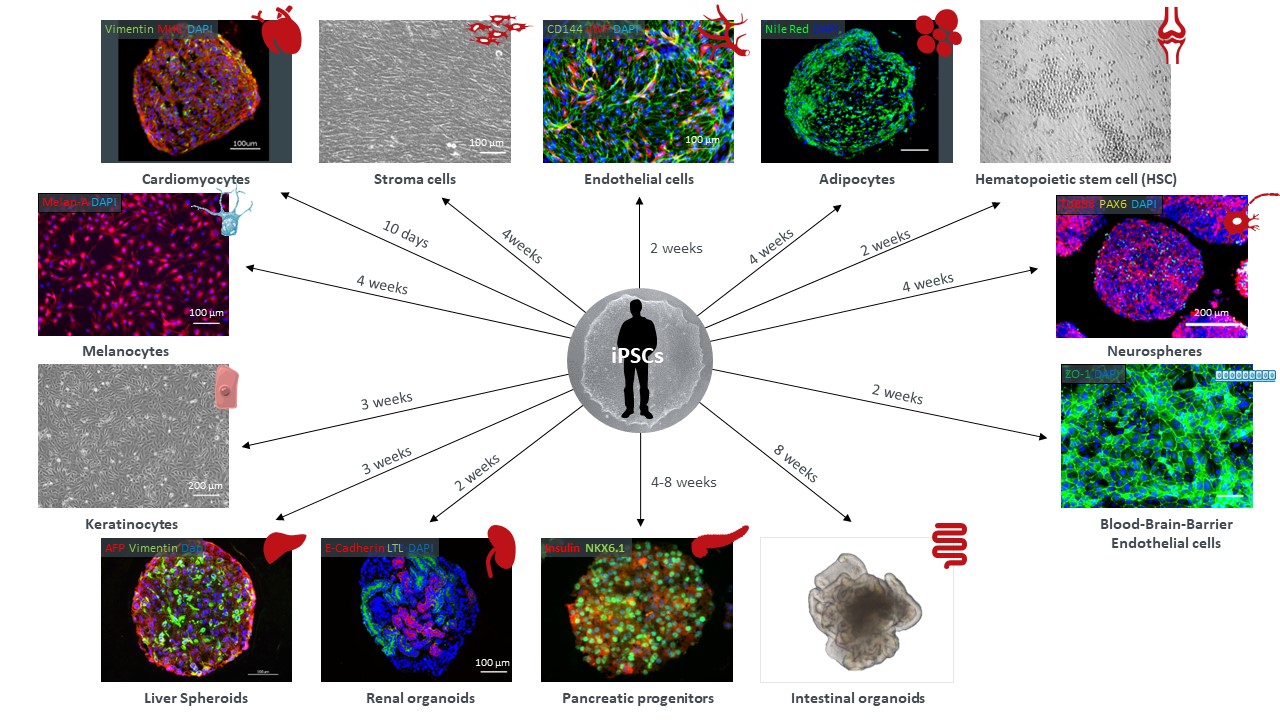
类器官是指在结构和功能上都类似来源器官或组织的模拟物,通过取特定器官的干细胞(iPS/ES),或者利用人的多能干细胞定向诱导分化,能获得微型的器官样的三维培养物,在体外模拟人体器官发育过程。
类器官,具有某一器官多种功能性细胞和组织形态结构的三维(3D)培养物,主要来源于人具有多项分化潜能的多能干细胞(包括人胚胎干细胞和人诱导多能干细胞iPSCs)或成体干细胞。人多能干细胞能分化为个体所有类型的细胞,在体外,经过诱导分化,模拟人体器官发育过程,能使人多能干细胞直接分化形成各种类器官;不同组织器官都存在内源组织干细胞,在维持各器官的功能形态发挥着重要作用。这些干细胞在体外一定的诱导条件下,可以自组织形成一个直径仅为几毫米的具有组织结构和多种功能细胞的三维培养物。器官芯片是获取两个或两个以上不同的类器官,并且放置在特定的培养芯片上进行共培养,能模拟人体的多个器官参与的生理学过程。
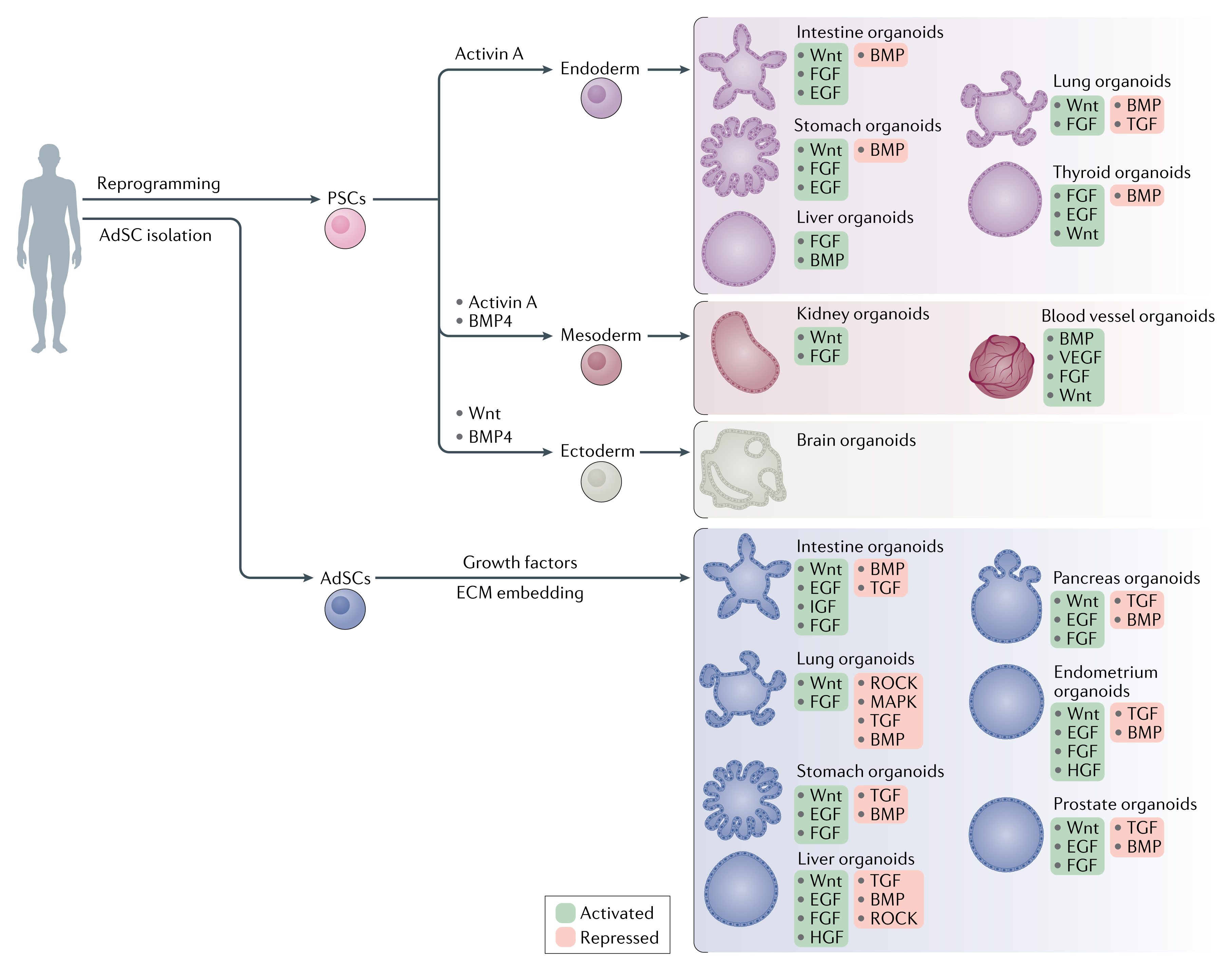
基于这一定义,可以发现类器官具备这样几个特征:
必须包含一种以上与来源器官相同的细胞类型;
应该表现出来源器官所特有的一些功能;
细胞的组织方式应当与来源器官相似。
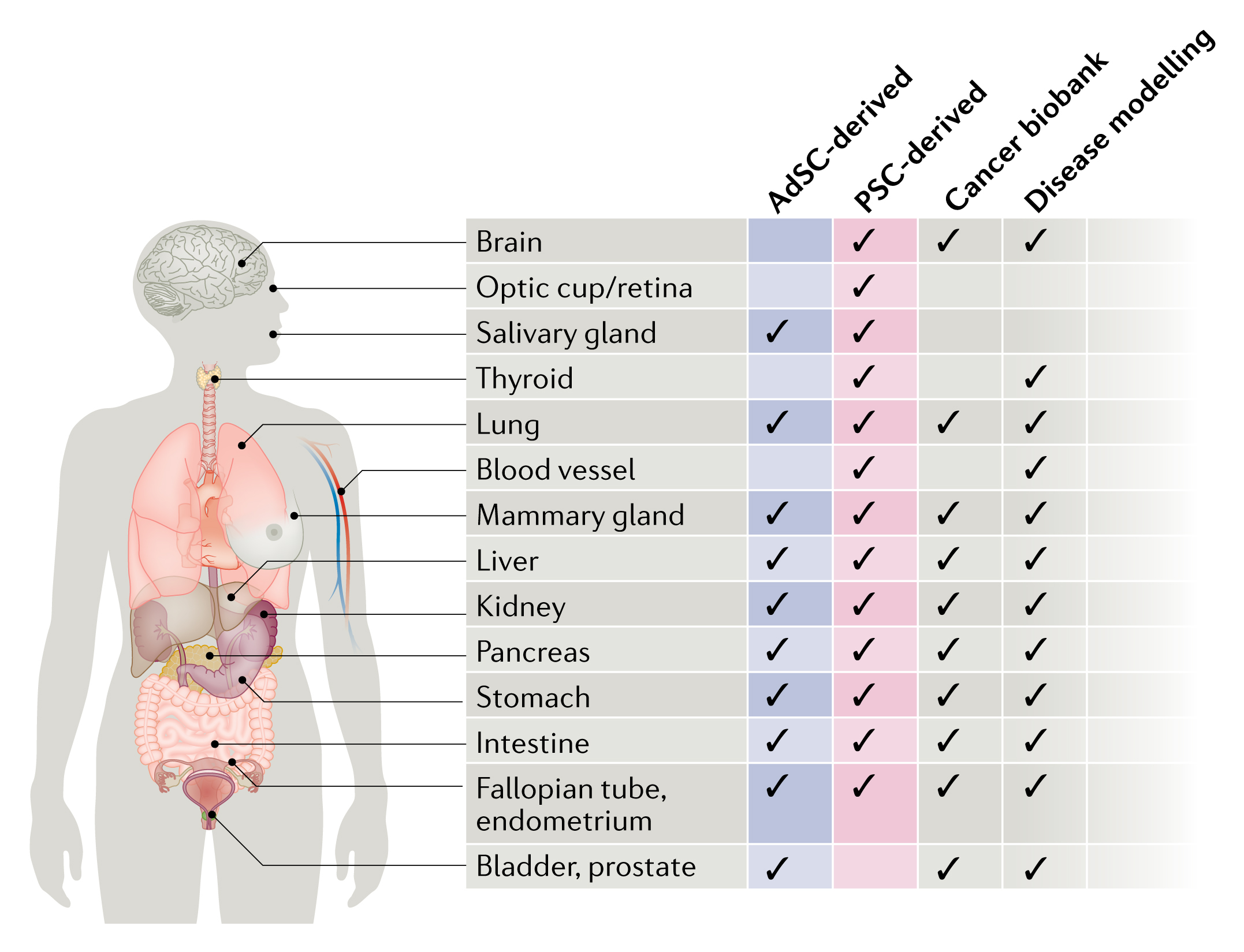
类器官作为一个新兴的技术,在科学研究领域潜力巨大,包括发育生物学、疾病病理学、细胞生物学、再生机制、精准医疗以及药物毒性和药效试验。与传统2D细胞培养模式相比,3D培养的类器官包含多种细胞类型,能够形成具有功能的“微器官”,能更好地用于模拟器官组织的发生过程及生理病理状态,因而在基础研究以及临床诊疗方面具有广阔的应用前景。
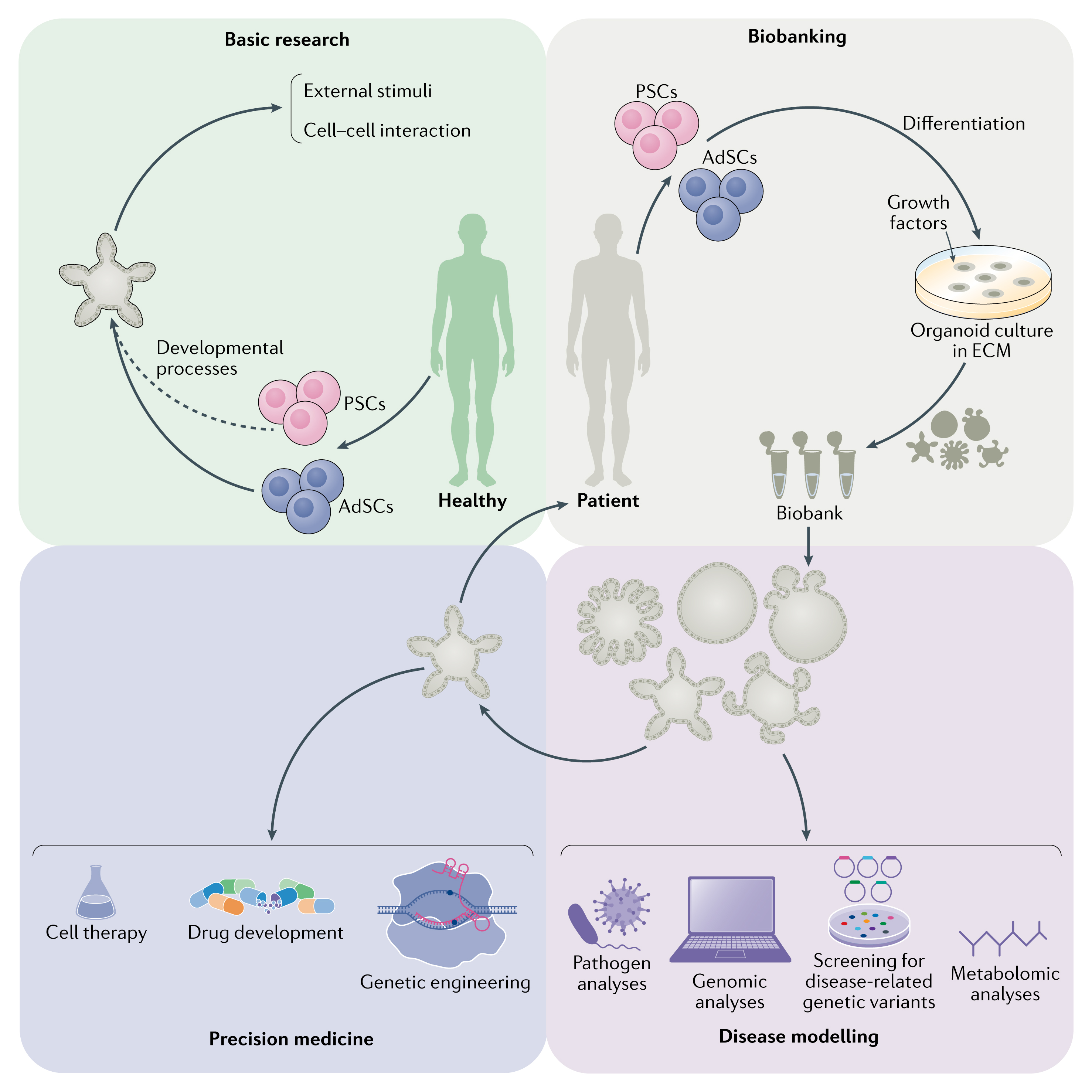
类器官培养使研究人体发育提供了不受伦理限制的平台,为药物筛选提供了新的平台,也是对现有2D培养方法和动物模型系统的高信息量的互补 。
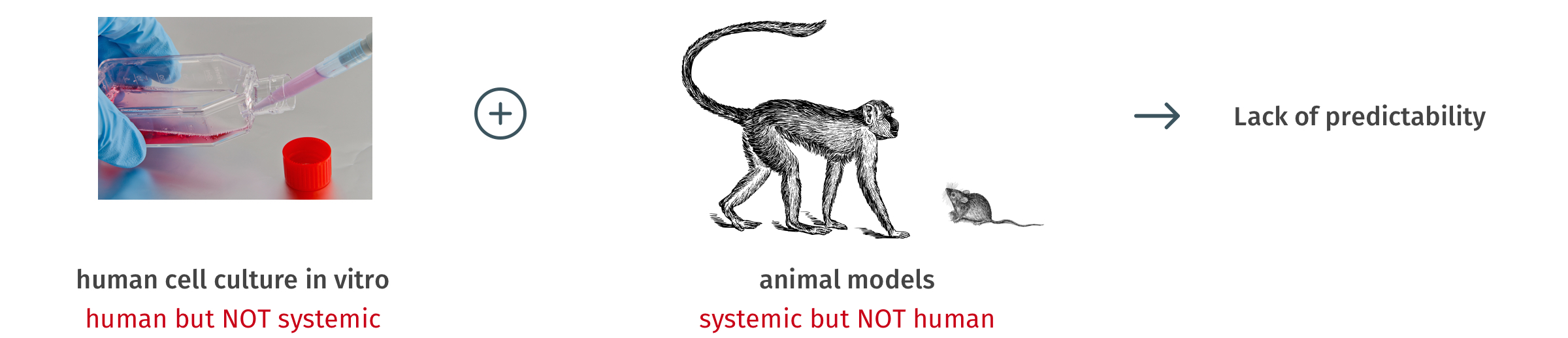

类器官可以模拟人体的内外环境和人体器官,帮助研究人员观测用药会对人体器官功能产生什么样的影响。在提倡精准医学和个体化治疗的时代,类器官研究比传统的二维细胞培养更具有针对性,并且可以区别不同癌症对于相同药物的反应。不仅如此,研究者还希望通过诱导多功能干细胞强大的再生潜能,体外生成新的器官或组织,然后移植入体内以替代损坏的组织器官。此外,类器官为获取更接近自然人体发育细胞用于细胞治疗成为可能。通过类器官繁殖的干细胞群取代受损或者患病的组织,类器官提供自体和同种异体细胞疗法的可行性,未来这一技术在再生医学领域也拥有巨大的潜力 。在精准医学应用中,患者衍生的类器官也被证明为有价值的诊断工具。在进行治疗之前,采用从患者样本来源的类器官筛查患者体外药物反应,旨在为癌症和囊胞性纤维症患者的护理提供指导并预测治疗结果。随着类器官培养系统以及其实验开发技术的不断发展,类器官应用到了各大研究领域。
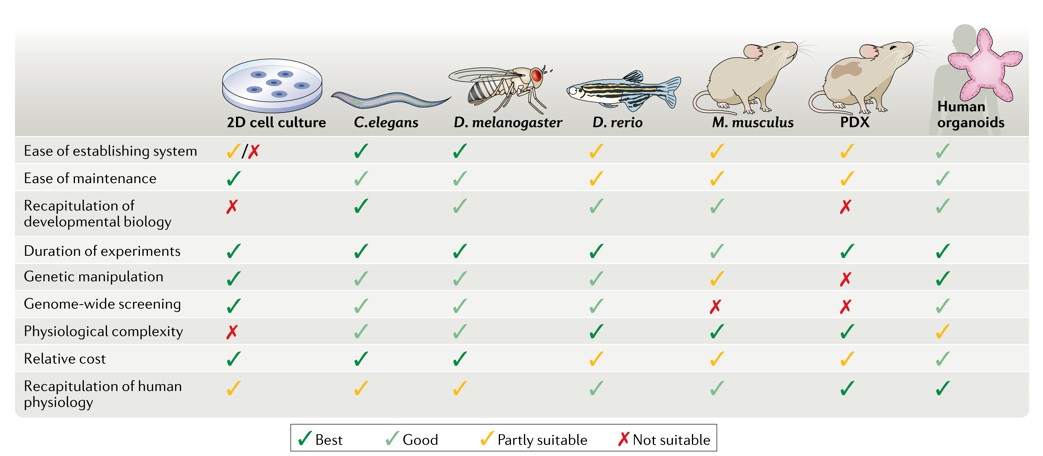
类器官培养的应用案例
类器官的应用举例---疾病模型
类器官的研究还可用于于疾病模型,如发育相关问题,遗传疾病,肿瘤癌症等。
通过使用患者的iPSCs可建立有价值的疾病模型,并能在体外模拟重现病人疾病模型;同时,类器官的建立可以实现对药物药效和毒性进行更有效、更真实的检测。由于类器官可以直接由人类iPSCs直接培养生成,相比于动物模型很大程度上避免了因动物和人类细胞间的差异而导致的检测结果不一致。
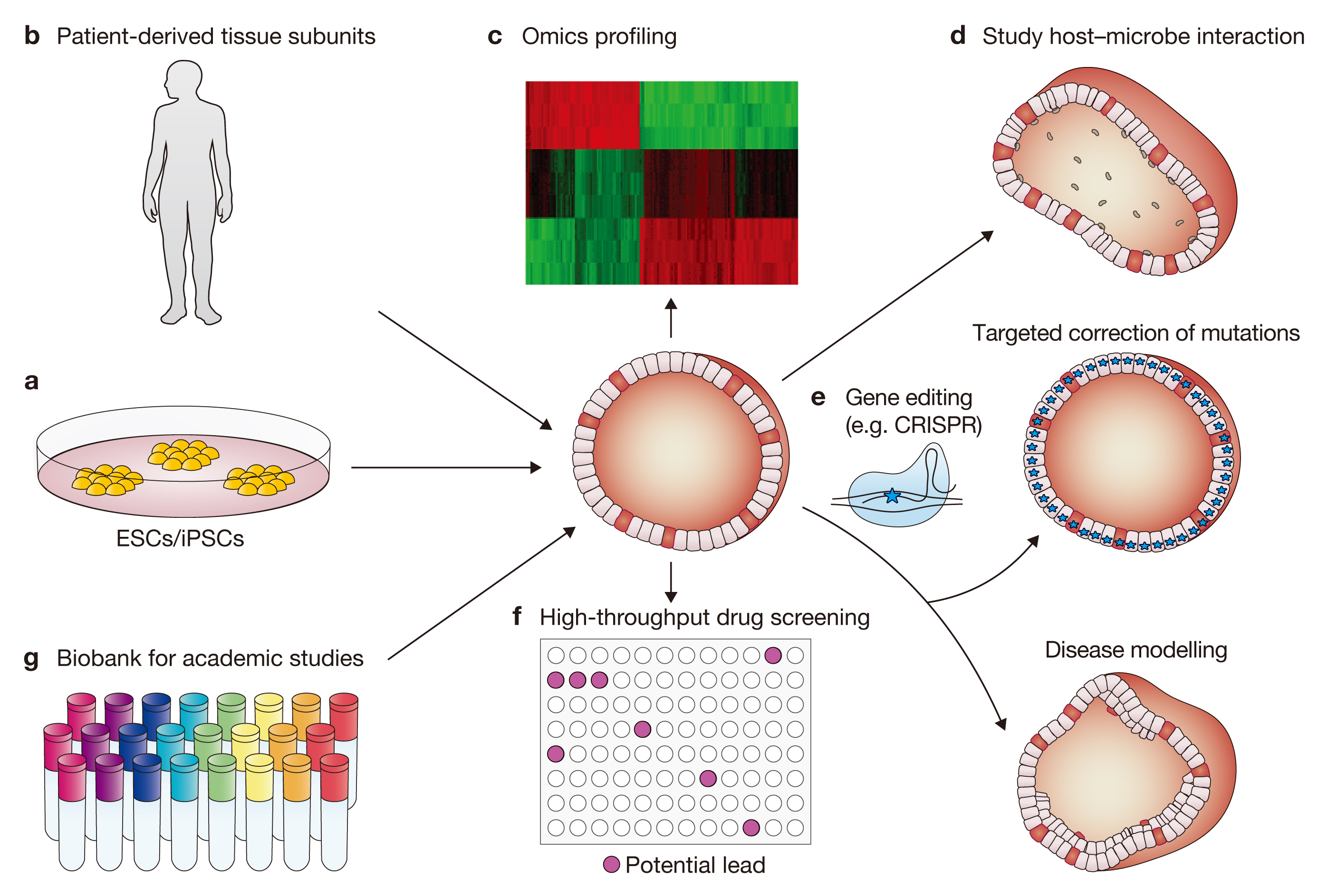
类器官的应用举例---药效和毒理测试
可以从患者来源的健康和肿瘤组织样品中建立类器官。与此同时类器官培养物可用于药物筛选,这可将肿瘤的遗传背景与药物反应相关联。来自同一患者健康组织的类器官的建立提供了通过筛选选择性杀死肿瘤细胞而又不损害健康细胞的化合物来开发毒性较小的药物的机会。自我更新的肝细胞类器官培养物可用于测试潜在新药的肝毒性(临床试验中药物失败的原因之一)。在该实施例中,药物B似乎最适合于治疗患者,因为它特异性杀死肿瘤类器官并且不引起肝毒性。
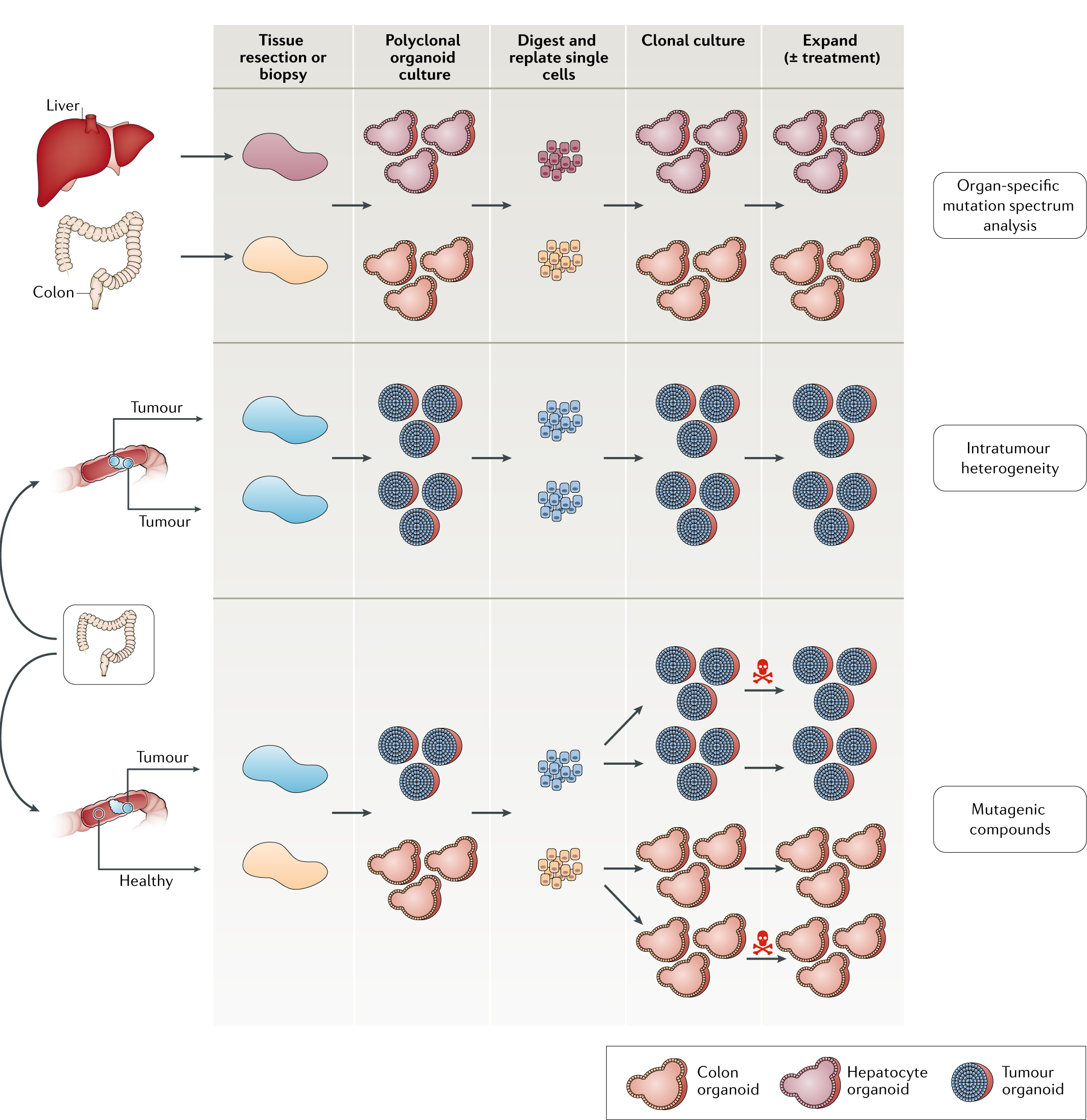
类器官的应用举例---重演肿瘤形成
类器官的培养和建立,可用于研究肿瘤生成过程中的突变过程,比如说,通过从同一肿瘤的不同区域培养无性繁殖的类细胞器,可以用来研究肿瘤内部的异质性。
来自不同健康器官的类器官的生长,然后对培养物进行全基因组测序,可以分析器官特异性突变谱。通过生长来自同一肿瘤不同区域的类器官,可以用于研究肿瘤内异质性。区域特异性突变谱可以通过类器官的全基因组测序来揭示。使用与上述相似的方法,可以利用类器官来研究特定化合物对健康细胞和肿瘤细胞突变谱的影响。
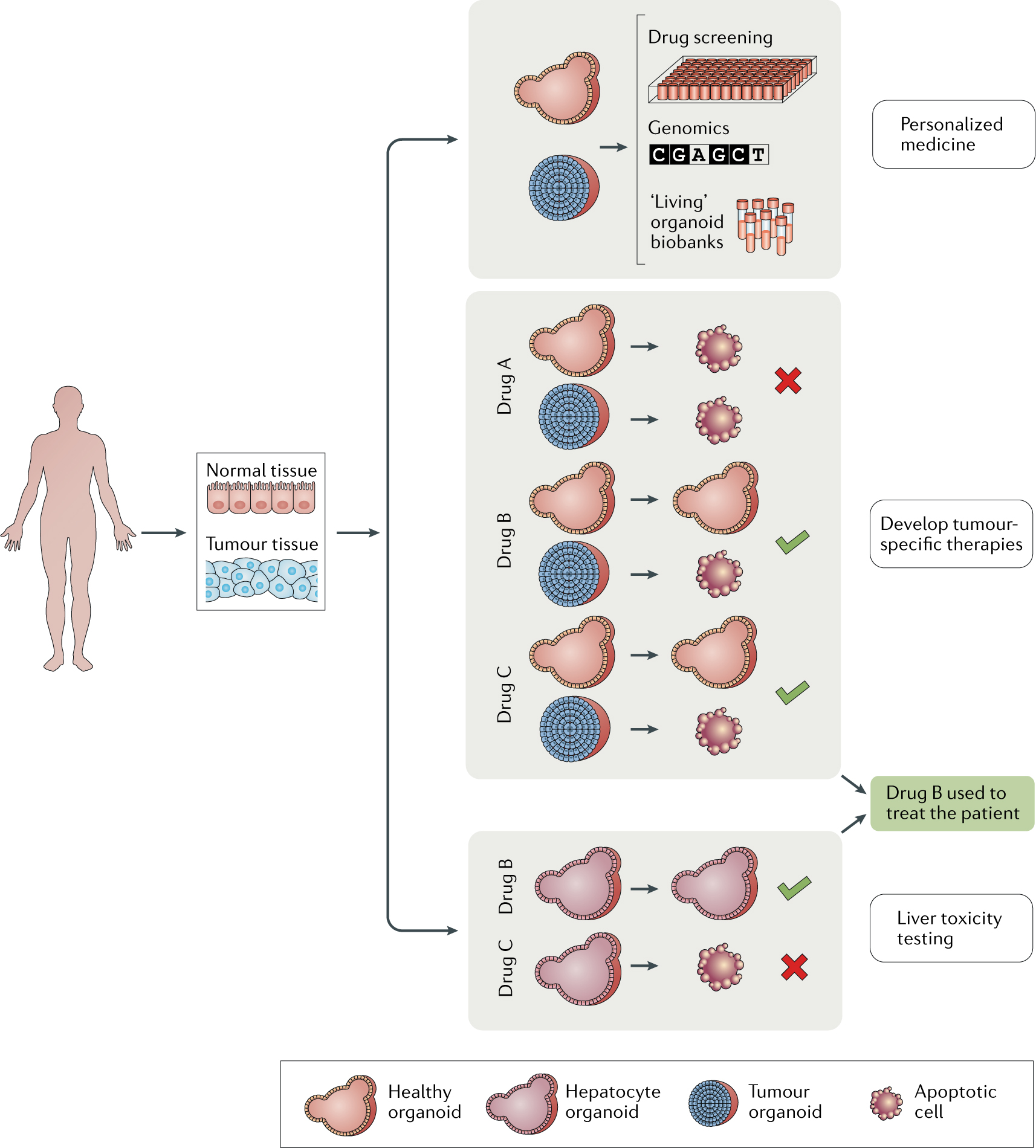
类器官的应用举例---肿瘤患者个性化医疗
有助于个性化治疗策略的设计,利用病变和正常的类器官来评估各种治疗方案。可以筛选多种活性药物和小化合物,设计更有效的用药方案。培养成熟的类器官还可以为器官再生和器官移植提供广泛的组织来源。对类器官进行基因操作来修复缺失的功能,并移植回到患者体内。
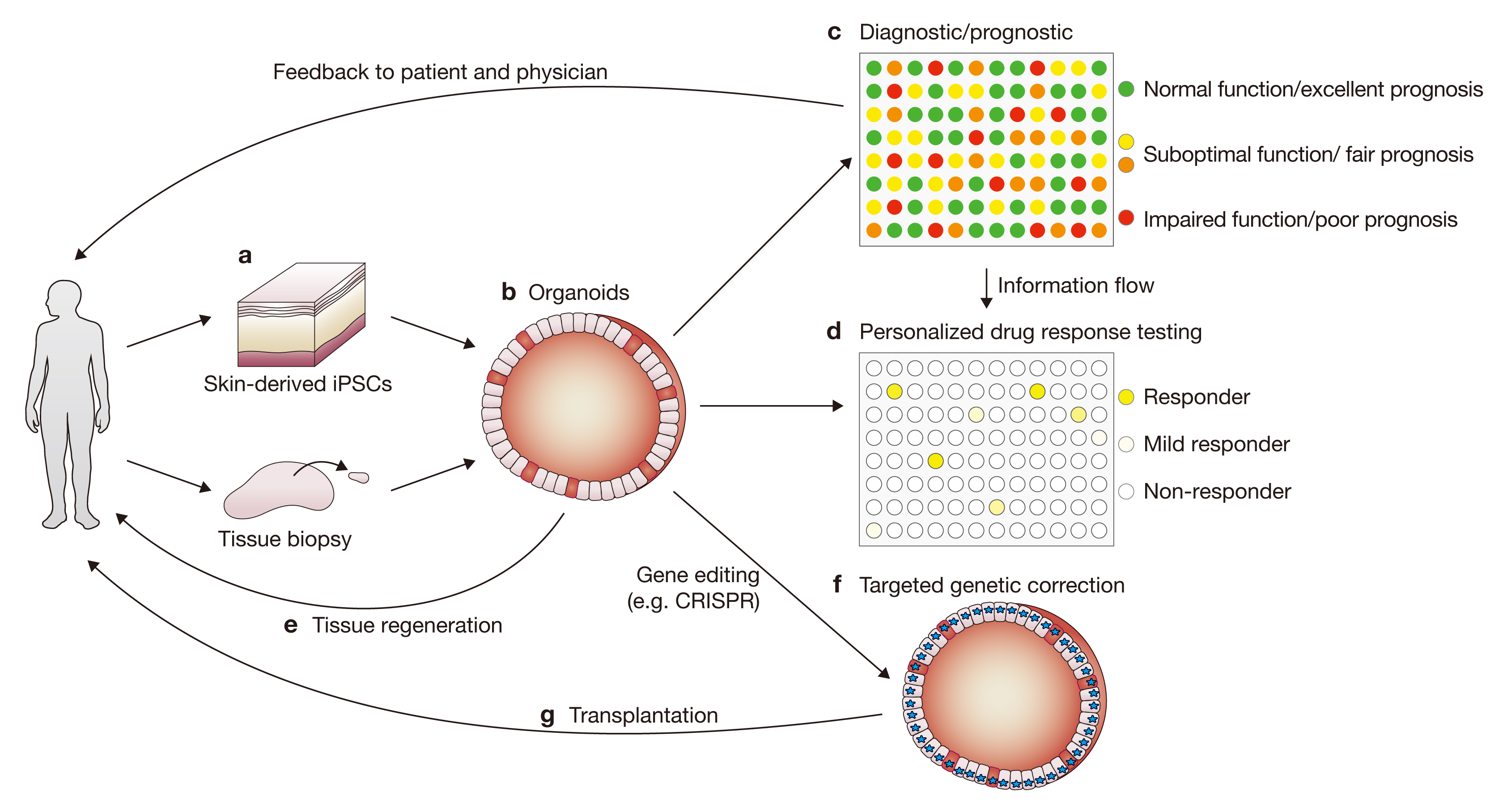
类器官的应用举例---类器官“生物Bank”
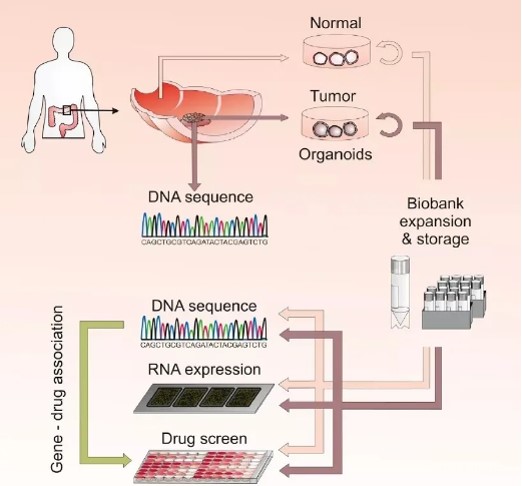
根据目前的研究进展,建立了活体类器官“生物bank”。其中,肿瘤来源的类器官在表型和基因上都与肿瘤相似。另外,肿瘤类类器官生物库使生理学相关的药物筛选成为可能。活体类器官生物库可用于确定类器官是否对个体患者的药物反应,具有预测价值。
从结直肠癌患者的健康组织和肿瘤组织中提取的三维有机组织培养物被用于高通量药物筛选,以确定可能促进个性化治疗的基因药物相关性
类器官培养的报道模型
肠类器官:
HansClever 课题组证实单一的Lgr5 +干细胞能够在体外持续增殖并自组装形成隐窝-绒毛样的小肠上皮结构。进一步的研究结果显示,单个成人Lgr5 + 干细胞也能在体外成功扩增成结肠类器官,将这种功能性的结肠上皮移植到硫酸葡聚糖诱导的急性结肠炎小鼠模型中可以修复其受损的结肠上皮。这提示利用单一成人结肠干细胞体外扩增进行结肠干细胞治疗是可行的。有学者还应用人诱导型多能干细胞( induced pluripotent stem cells,iPSCs) 直接定向分化为小肠组织的方法明确了Wnt3a 蛋白和成纤维细胞生长因子4 是后肠特定分化所必需的物质,而且,这种iPSCs体外构建的人体肠道组织中存在的小肠干细胞,也具有小肠特有的吸收和分泌功能。这有助于未来人肠道疾病药物的设计研究,可大大提高了药物利用率。目前,已有学者构建了小鼠小肠3D 类器官来进行P-糖蛋白抑制剂的筛选,为P-糖蛋白介导的药物转运研究提供了强有力的工具。
肝类器官:
2013 年,Takebe 等将人多能干细胞来源的肝细胞、人间充质干细胞和人内皮细胞混合后在基质胶中培养,发现3 种细胞自组装成3D 化肝芽,将该肝芽移植到丙氧鸟苷诱导肝脏衰亡的TKNOG 小鼠体内后发现这种肝芽可以连接小鼠肠系膜血管,小鼠也出现了人类特有的药物代谢过程。这为肝脏器官发生的研究提供了有益尝试。大型哺乳动物的类器官再造工程也许能加速人类器官移植治疗和疾病致病机制研究的进展。2015 年,Nantasanti 等利用狗的肝脏干细胞构建了可分化为功能性肝细胞的肝类器官模型,能用于铜潴留症的治疗。猫被认为是非常适用于研究人类代谢性疾病的模型,所以利用猫的胆道组织构建肝类器官,可能是原发性肝胆疾病研究及药物筛选的有益工具,但至今也未见利用猫建立长期保持基因稳定的肝脏干/祖细胞培养体系的报道。
胰腺类器官:
有学者发现,当控制骨形态发生蛋白碱性成纤维细胞生长因子、激活素A 和Wnt3a 的表达水平或使用一些小分子化合物进行干预时,可以控制内胚层细胞向特定的方向分化,最终形成胰腺。目前,构建胰岛类器官的主要方法包括利用各种干祖细胞产生胰岛样细胞群和利用各种来源的胰腺细胞悬液或胰腺组织块自组装成拟胰岛体。2011 年,Saito 等将人iPSCs 和胚胎小鼠胰岛细胞体外共培养,最后形成能够产生胰岛素的不成熟细胞群,该细胞群由胰岛α 细胞包绕中央的β 细胞构成,这种结构和成年鼠胰岛相似,将其移植到链脲菌素诱导的高血糖小鼠模型中后发现小鼠血糖水平得到极大改善。而进一步的体内实验研究还需要关注如何规避免疫反应、促进再血管化、促进类器官分化发育等问题,在这方面,Sabek 等提出制备纳米腺体来促进胰岛发挥作用,这种纳米腺体是运用3D 打印技术制作可吸收聚合物胶囊包裹胰岛样细胞团形成的,这可能是未来胰岛类器官应用的一种思路。
脑类器官:
近来,谱系重编程技术为获取特异性种子细胞提供了新的途径。Lancaster 等通过加入不同生长因子的方法将人类胚胎干细胞( embryonic stem cell,ESC) 和iPSC 在神经培养基3D 培养出了与9 ~ 10周胚胎大脑类似的“类大脑”,此类迷你大脑具备人类大脑发育初期的一些主要区域,也出现了背侧皮层、腹侧前脑等可辨认的特征,但由于缺乏一些特定的特征,如小脑、海马状突起等,这些区域无法应用于干细胞模型。之后,该研究者利用小颅畸形患者的皮肤成纤维细胞诱导形成了患者特异性iPSC 细胞系,并应用后者构建了小颅畸形脑类器官模型,通过对照实验发现,正常ESC和该iPSCs 在类器官形成上并没有明显差异,但是后者形成的类器官中有大量未成熟的神经元分化,这为大脑发育紊乱类疾病的研究提供了一定的思路。2015年Kirwan 等应用人iPSC 体外构建了人大脑皮层神经网络,能够模拟人体内皮层网络的发育和功能,这表明可以在体外通过构建大脑类器官来进行人类前脑神经网络生理学机制的研究。
前列腺类器官:
2014 年,研究人员首次在实验室利用来自转移性前列腺癌患者的活检标本和去势抵抗性前列腺癌( castration-resistant prostate cancer,CRPC) 患者的循环肿瘤细胞成功培育出7 个前列腺癌类器官,这些前列腺癌类器官以及从中获得的肿瘤移植物的组织结构及基因突变谱与患者转移灶样本高度相似。Nicholson 等[21]也应用类器官培养技术成功在体外构建患者来源的异种移植物模型,相比于人源性肿瘤组织异种移植及基因工程鼠模型,这种新型的患者来源的类器官能更好地代表CRPC 等高级别前列腺癌,还能代表前列腺癌的庞大临床疾病谱,而这种疾病谱是目前仅有的前列腺癌细胞系无法代表的,因而在前列腺癌药物筛选和个体化治疗中展现出巨大的应用前景。
类器官串联培养系统--- HUMIMIC的技术方案:
多器官串联培养,在没有病人的情况下测试病人
类器官串联芯片培养系统包括控制单元和芯片,控制单元能够模拟人体内生理环境,包括温度、压力、真空度、微流道循环频率、时间等参数,芯片有不同的微流道设计,针对不同的器官可以单独设置提供相应的培养条件,提供精准的培养和分化环境。类器官串联芯片培养系统可提供不同类器官的串联共培养方案,避免单一类器官无法模拟人体复杂生理学条件下器官相互通讯交流的不足。通过类器官模拟人类器官组织的生理发育过程,应用于疾病模型、肿瘤发生、以及药物安全性、有效性、毒性、ADME等方面的评估,旨在减少和取代实验室动物测试,简化人体临床试验。
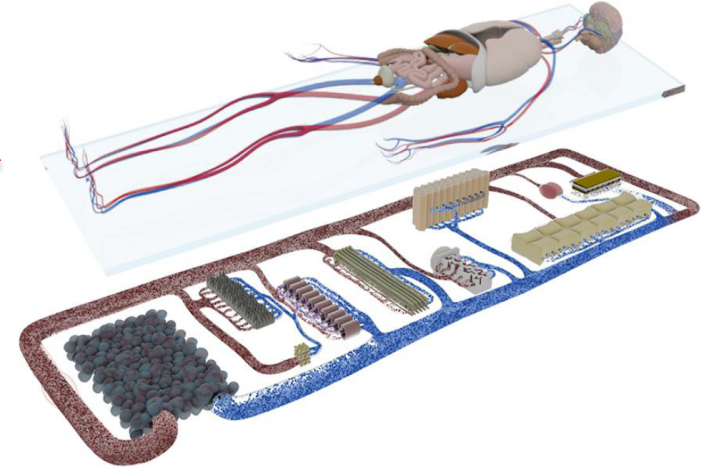
为获取更高相关与准确的测试结果,我们开发了人体器官模型的自动芯片测试:
配备具有指示相关性的器官模型的芯片,以能够在接触生物体之前检测其安全性和有效性;
最终为芯片配备患者自身相关病变器官的亚基,以评估整个个性化治疗的效果;
人体生理反应往往涉及更多介质循环和不同组织间相互作用,多器官芯片才能全面反映出机体器官功能的复杂性、完整性以及功能变化,一个相互作用的系统才能更好的模拟整个系统中器官和组织的不同功能。可提供不同类器官的串联培养解决方案,避免单一类器官无法模拟人体复杂生理学条件下器官相互通讯交流的不足。把多种不同器官和组织培养在芯片上,然后通过微通道连接起来,集成一个相互作用的系统,从而模拟人体中的不同功能器官的交流通讯和互相作用。
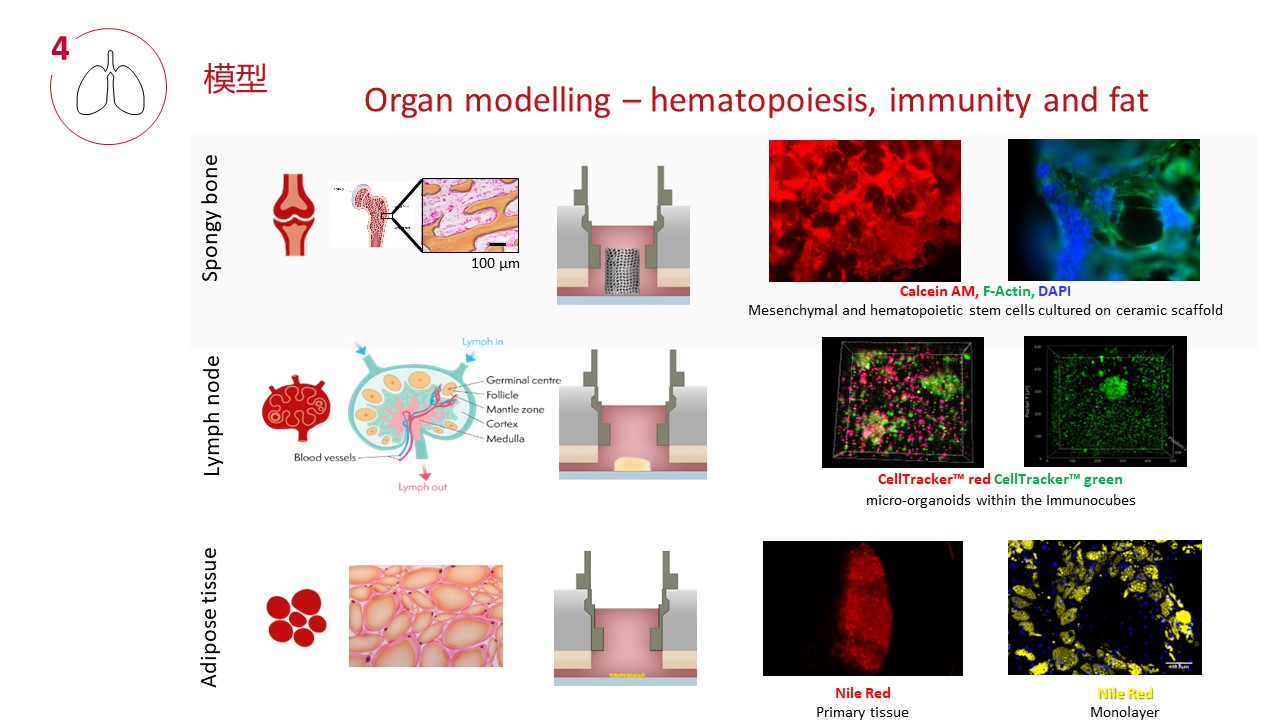
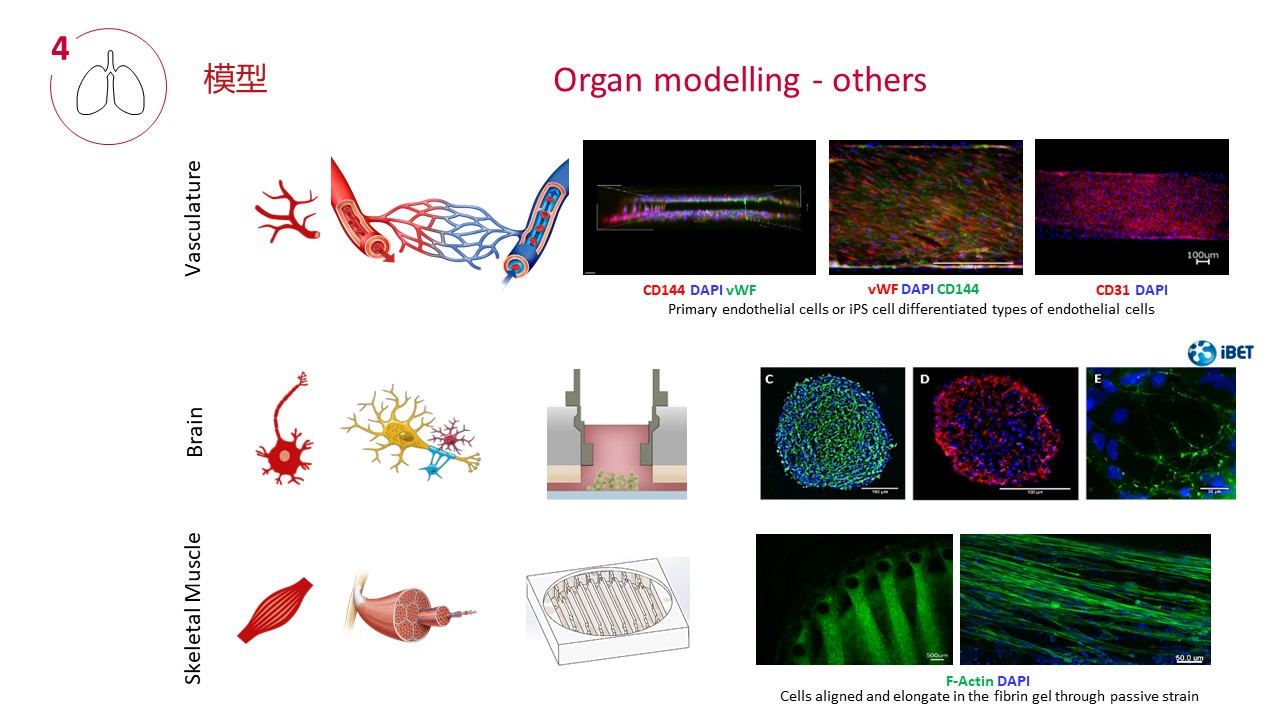
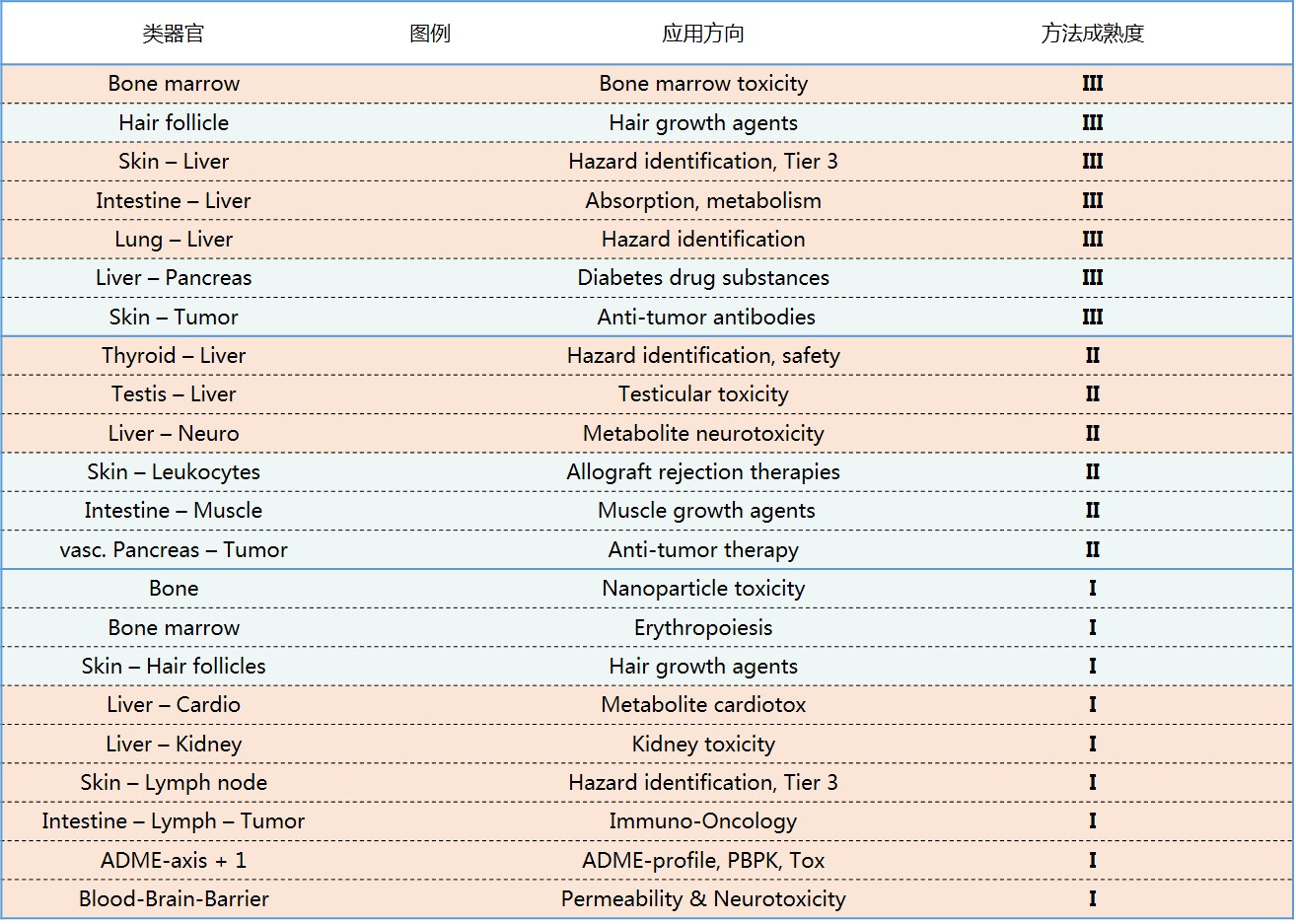
TissUse专有的商用MOC技术支持的器官培养物的数量范围从单个器官培养到支持复杂器官相互作用研究的器官数量,包括单器官、二器官、三器官和四器官培养的商业化的平台。成功的案例包括:肝脏、肠、皮肤、血管系统、神经组织、心脏组织、软骨、胰腺、肾脏、毛囊、肺组织、脂肪组织、肿瘤模型和骨髓以及各自的多器官串联组合方案。
德国TissUse公司专注于类器官培养系统研究22年,推出的HUMIMIC类器官串联芯片培养系统,得到FDA的推荐,可提供不同类器官的串联培养解决方案,避免单一类器官培养无法模拟人体器官相互通讯关联的缺陷,同时也提供相关的技术方案和后续方法试剂支持,属于国际上少有的“Multi-Organ-Chip” 和“Human-on-a-chip”的方案提供者。相关方案已被广泛应用于药物开发、化妆品、食品与营养和消费产品等多个领域.
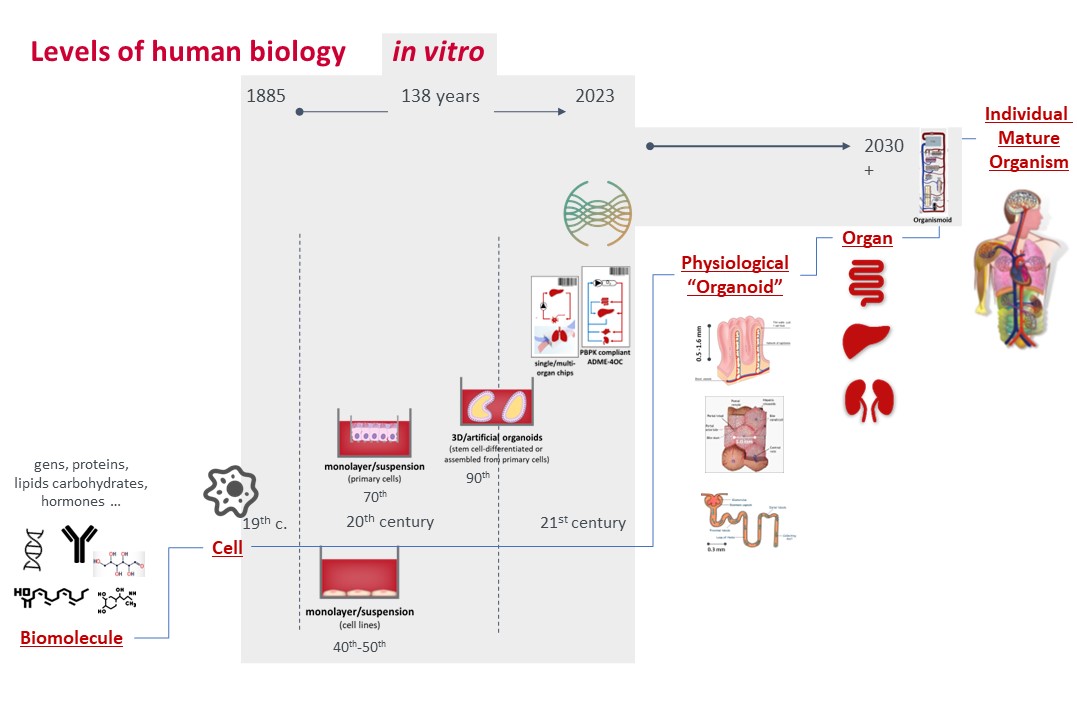
类器官串联培养系统---HUMIMIC系统
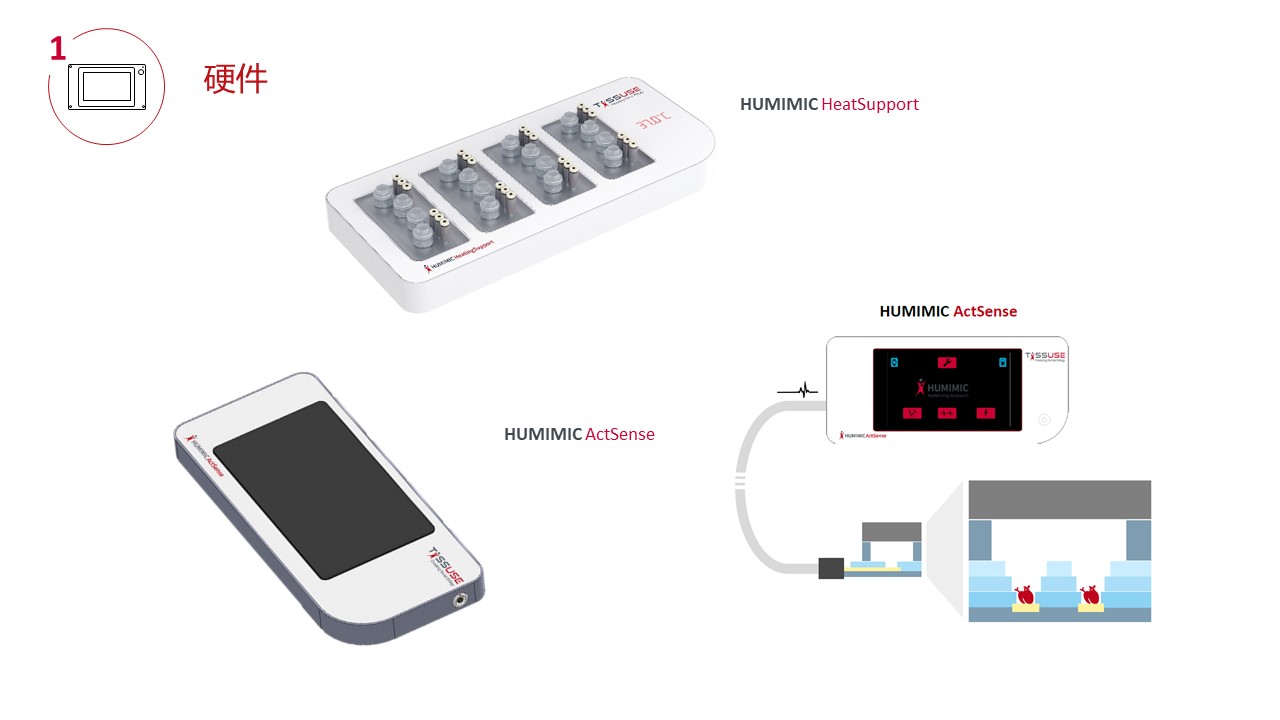
一、专业化的硬件(控制单元)
主机(控制单元)是一个台式设备,能够控制类器官培养环境,包括温度、压力、真空度、微流道循环频率、时间等参数;
7寸触摸显示器,控制面板可以在整个过程中对每个多器官芯片分别进行调节,无需外接电脑,软件操控友好;
可以自主设置每个器官芯片的培养条件,包括温度、压力、真空度、微流道循环频率、时间等参数;
可串联培养2个不同(或相同)、3个不同的、4个不同的类器官;
3个连接拓展口,用于连接其他设备;
同时操控高达8个Chip3 / Chip3 plus,4个Chip2 /Chip4或这些的组合;

二、类器官芯片
芯片有不同的微流道设计,针对不同的器官可以单独设置提供相应的培养条件,提供精准的培养和分化环境;
芯片的泵腔内的柔性膜通过连接的管道,受到压力或真空的作用,在微流道之中产生脉动体流;
二联类器官芯片可以在一个芯片上串联培养2个不同(或相同)的类器官;
三联类器官芯片可以在一个芯片上串联培养3个不同的类器官;
四联类器官芯片可以在一个芯片上串联培养4个不同的类器官;

三、服务方案(细胞、试剂,诱导方案)


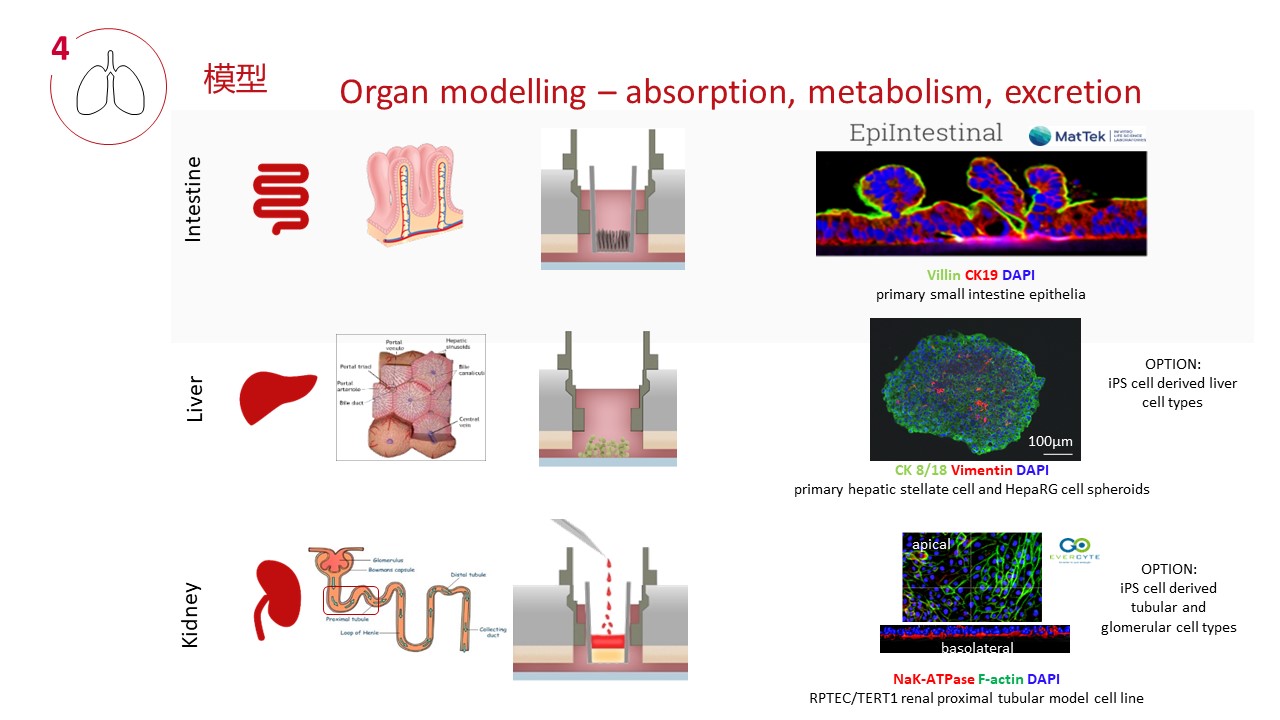
四、器官模型和串联培养技术
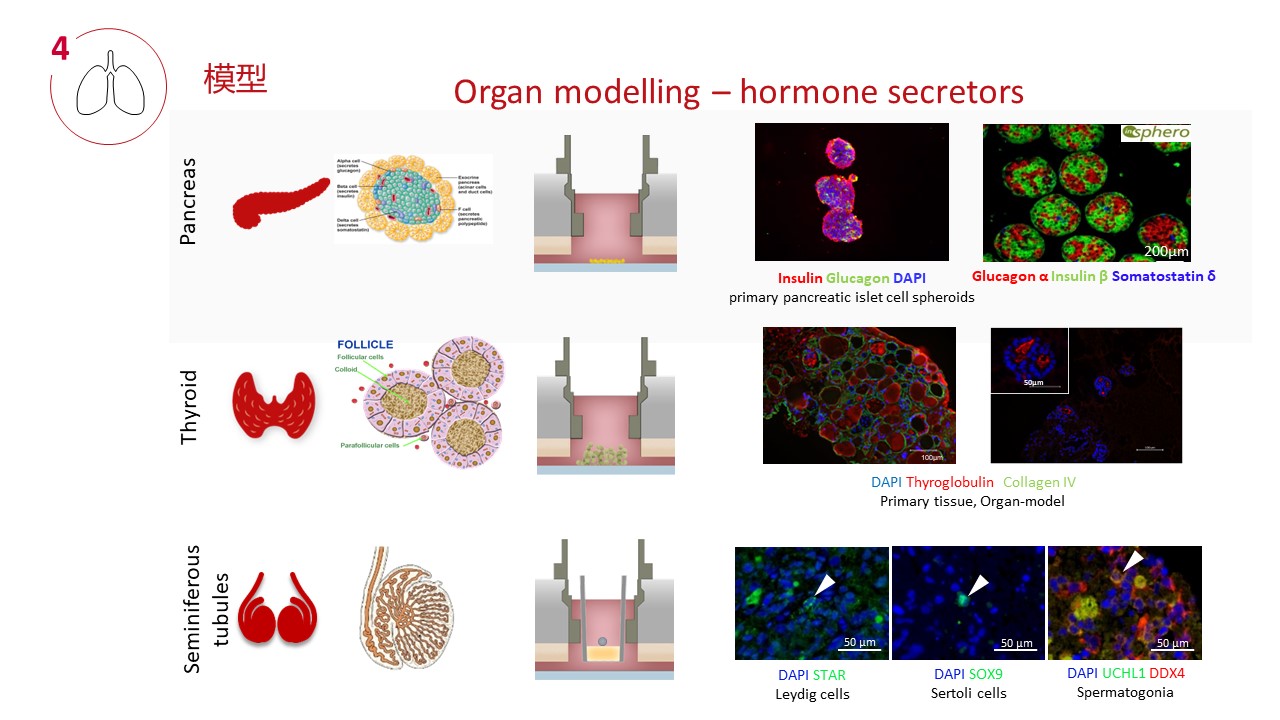


类器官串联培养系统---HUMIMIC的应用案例
1、神经和肝脏类器官的串联共培养(柏林工业大学)—二联器官共培养的药物敏感性
2015, Journal of Biotechnology,
A multi-organ chip co-culture of neurospheres and liver equivalents for long-term substance testing
目前用于药物开发的体外实验平台无法模拟人体器官的复杂性,而人类和实验室动物的系统差异巨大,因此现有的方案都不能准确预测药物的安全性和有效性。德国、葡萄牙和俄罗斯的研究团队通过TissUse GmbH公司的微流控多器官芯片(MOC)平台,测试毒物对多器官的作用,揭示了基于微流控的多器官串联共培养能够更好的模拟人体的生理学环境。在体外培养条件下,由于氧气和营养供应有限,类器官培养往往会随着时间的推移而去分化。然而微流控系统中通过持续灌注培养基,更好地控制环境条件,如清除分泌物和刺激因子,并且培养基以可控流速通过,以模拟血流产生的生物剪切应力,因此类器官培养物可以保持良好的生长状态。

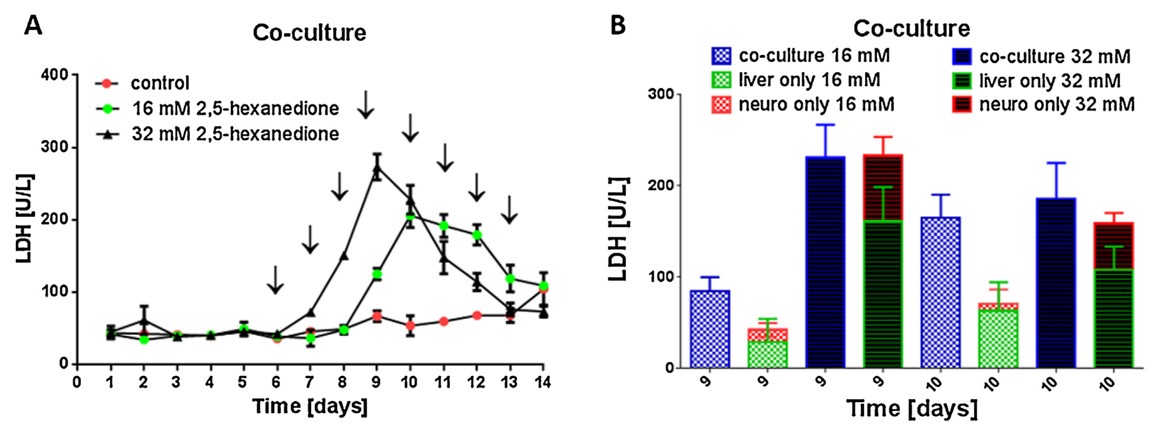
双器官串联芯片(2-OC)能够串联共培养人的神经球(NT2细胞系)和肝脏类器官(肝HepaRG细胞和肝HHSteC细胞)。在持续两周的实验中,反复加入神经毒剂2,5-己二酮,引起神经球和肝脏的细胞凋亡。跟单器官培养相比,串联共培养对毒剂更敏感。因此,多器官串联共培养在临床研究中可以更准确地预测药物的安全性和有效性。推测这是因为一个类器官的凋亡信号导致了第二个类器官对药物反应的增强,这一推测得到了实验结果的支持,即串联共培养的敏感性增加主要发生在较低浓度药物中。
2、心脏肝脏骨骼皮肤的串联共培养(哥伦比亚大学)—四联器官共培养的复杂通讯模型
哥伦比亚大学的科学家也开发了一种多器官串联芯片,建立了串联共培养心脏、肝脏、骨骼、皮肤的技术,发表于2022年的Nature Biomedical Engineering,中通过血液循环串联培养4个类器官,保持了各个类器官的表型,还研究了常见的抗癌药阿霉素对串联芯片中的类器官以及血管的影响。结果显示药物对串联共培养类器官的影响与临床研究结果非常相似,证明了多器官串联共培养能够成功的模拟人体中的药代动力学和药效学特征。
“最值得注意的是,多器官串联芯片能够准确的预测出阿霉素的心脏毒性和心肌病,这意味着,临床医生可以减少阿霉素的治疗剂量,甚至让患者停止该治疗方案。“
Gordana Vunjak-Novakovic, Department of Biomedical Engineering, Columbia University
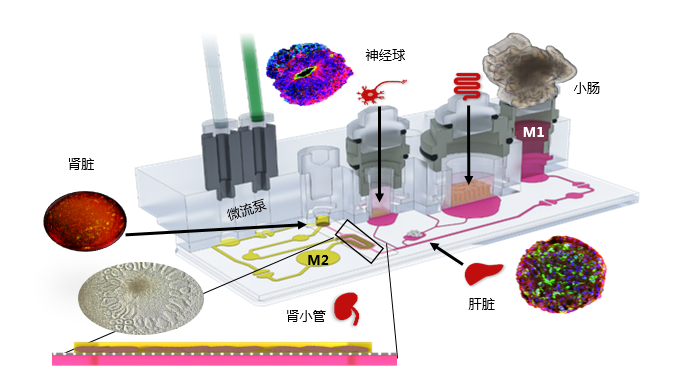
3、胰岛和肝脏类器官的串联共培养(阿斯利康)—二联器官共培养的反馈通讯
2017, Nature Scientific Reports,
Functional coupling of human pancreatic islets and liver spheroids on-a-chip: Towards a novel human ex vivo type 2 diabetes model
人类系统性疾病的发生过程都是通过破坏两个或多个器官的自我平衡和相互交流。研究疾病和药疗就需要复杂的多器官平台作为体外生理模型的工具,以确定新的药物靶点和治疗方法。2型糖尿病(T2DM)的发病率正在不断上升,并与多器官并发症相关联。由于胰岛素抵抗,胰岛通过增加分泌和增大胰岛体积来满足胰岛素不断增加的需求量。当胰岛无法适应机体要求时,血糖水平就会升高,并出现明显的2型糖尿病。由于胰岛素是肝脏代谢的关键调节因子,可以将生产葡萄糖的平衡转变为有利于葡萄糖的储存,因此胰岛素抵抗会导致糖稳态受损,从而导致2型糖尿病。过去已经报道了多种表征T2DM特征的动物模型,但是,从动物实验进行的研究往临床上转化的效果不佳。更重要的是,目前使用的药物,虽然能缓解糖尿病症状,但对疾病进一步发展的治疗效果有限。
胰腺和肝脏是参与维持葡萄糖稳态的两个关键器官,为了模拟T2DM,阿斯利康(AstraZeneca)的科学家利用TissUse GmbH公司的微流控多器官芯片(MOC)平台,通过微流控通道相互连接,建立一个双器官串联芯片(2-OC)模型,实现芯片上胰腺和肝脏类器官的串联共培养,在体外模拟了胰腺和肝脏之间的交流通讯。

建立串联共培养类器官(胰岛+肝脏)和单独培养类器官(仅胰岛或肝脏),在培养基中连续培养15天,串联共培养显示出稳定、重复、循环的胰岛素水平。而胰岛单独培养的胰岛素水平不稳定,从第3天到第15天,降低了49%。胰岛与肝球体串联共培养中,胰岛可长期维持葡萄糖水平,刺激胰岛素分泌,而单独培养的胰岛,胰岛素分泌显著减少。胰岛分泌的胰岛素促进了肝球体对葡萄糖的利用,显示了串联共培养中类器官之间的功能性交流。在单独培养中的肝球体中,15天内循环葡萄糖浓度稳定维持在~11 mM。而与胰岛共培养时,肝球体的循环葡萄糖在48小时内降低到相当于人正常餐后的水平度,表明胰岛类器官分泌的胰岛素刺激了肝球体摄取葡萄糖。
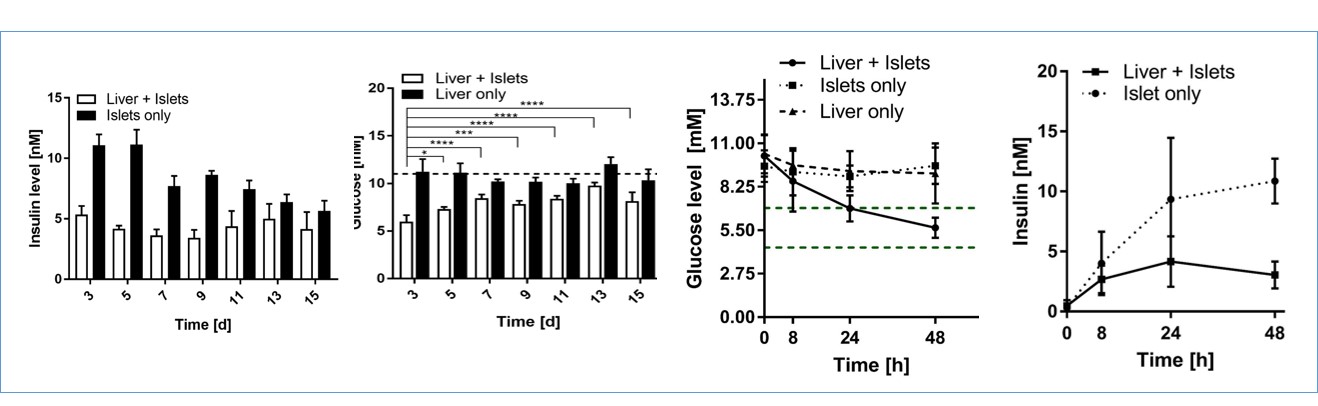
4、肺肿瘤和皮肤类器官的串联共培养(拜耳)—抗体药物对肿瘤和正常器官的影响
针对EGFR抗体的药物在癌症治疗中被广泛应用。然而,抗癌药物的使用量与皮肤不良反应成正比相关,皮肤毒性是上皮生长因子受体(EGFR) 靶向治疗中最常见的副作用。但是对于后者的预测目前的方法均无法实现。
双器官串联芯片(2-OC)模型,实现芯片上皮肤和肿瘤的共培养,用于模拟重复给药的剂量实验,同时还生成安全性和有效性的数据,可以在非常早的阶段检测到西妥昔单抗cetuximab对皮肤的几个关键副作用。这种体外分析能够在临床表现之前预评估毒性副作用,可以替代动物试验,有望成为评价EGFR抗体和其他肿瘤药物治疗指数的理想工具。
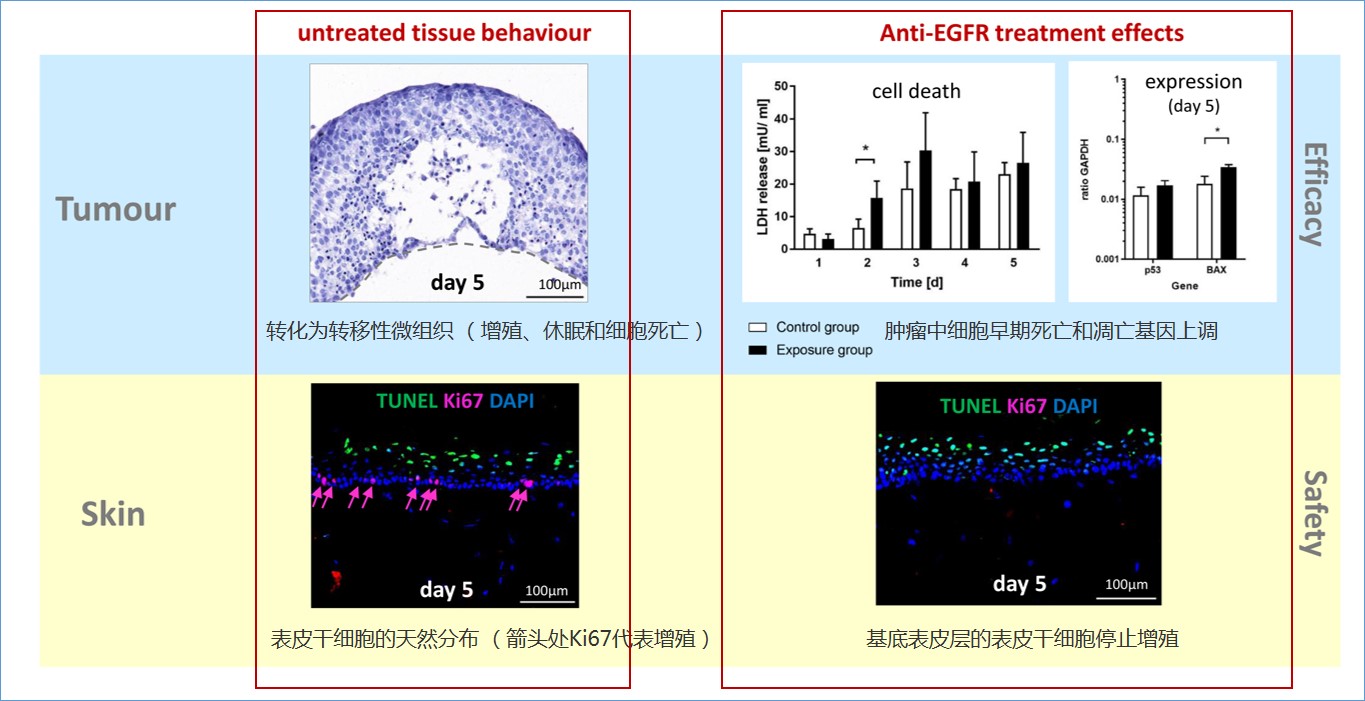
5、皮肤-肝脏类器官的串联共培养(拜尔斯道夫公司)—评估化妆品不同的给药途径
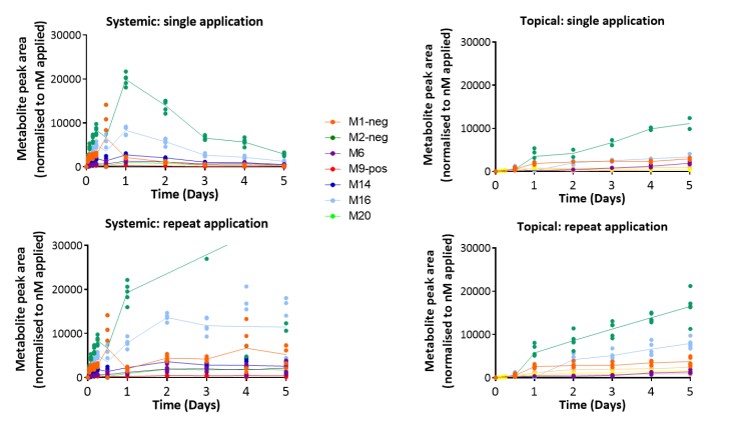
一种独特的基于芯片的组织培养平台已经开发出来,使化妆品和药物对一套微型人体器官的影响测试成为可能。这种“人-片”平台旨在生成可复制的、高质量的人体物质安全性预测体外数据。被测物质进入表皮或在表皮内代谢,然后泵入肝脏并激活相应的CYPs。因此,在肝脏和皮肤的联合培养中,多器官芯片是一种有前途的体外方法,用于全身和局部剂量的化妆品和药物。
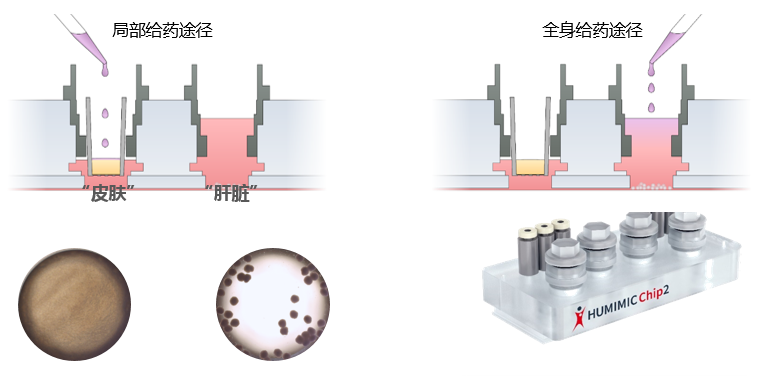
皮肤等效物的培养整合在一个系统中。芯片上的微泵使代谢运输和附加的生理剪切应力成为可能。肝脏和皮肤等效物存活10天,并显示紧密连接和特异性转运蛋白的表达。每天服用咖啡因、维甲酸和倍他米松-21-戊酸,持续7天,以研究已知可被皮肤和肝脏代谢的化合物的作用。将表面敷于表皮的效果与直接敷于培养基的效果进行比较,分析对皮肤渗透和代谢的影响。对肝脏和皮肤等价物进行代谢酶、转运体、分化标记物的表达和活性分析。结果显示,在蛋白水平和mRNA水平上,根据不同物质处理,ⅰ、ⅱ期酶均有本构性和诱导性表达。因此,在肝脏和皮肤的联合培养中,多器官芯片是一种有前途的体外方法,用于全身和局部剂量的药物和化妆品。
6、肺类器官在芯片上的培养(菲莫国际)_—空气环境对呼吸道的影响
使用类人肺模型研究吸入气溶胶的沉积和吸附,从而使体外人体呼吸毒性的数据更加准确和可预测。目前的体外气溶胶暴露系统通常不能模拟这些特性,这可能导致在体外生物测试系统中交付非现实的、非人体相关的可吸入试验物质剂量。模拟和研究体外气溶胶暴露装置-吸入器可主动呼吸、操作医用吸入器,或吸吸烟草制品。此外,它可以填充从人类呼吸道不同区域分离的三维上皮细胞。包括口腔、支气管和肺泡细胞培养物的气溶胶传递和相容性的概念的研究,将其应用于测试系统,吸入产生的生理条件下,测试表现在人的呼吸道的方式。这种方法的优点是,它无需花费昂贵、耗时和具有科学挑战性的工作来确定体内提供的剂量,默认情况下,适用于任何测试烟草燃烧产生的气体和任何测试成分。
此外,通过功能和结构上培养人的呼吸道器官模型,该系统消除了在处理呼吸道不同区域时重复暴露与吸烟环境,并能够测试任何相关的呼吸模式或行为。由于该系统能够自行产生或取样测试气溶胶,且其方式与人类呼吸道的做法高度相似,因此消除了在外部测试大气产生或取样过程中引入实验人工制品的风险。
通过建立类器官培养和鉴定平台,培养人肺类器官模型,研究烟草(包括电子烟)燃烧后的气体对人体内健康的影响,从而领导烟草行业的一场技术变革,以创造一个无害烟的未来,并最终以无害烟产品取代香烟,从而造福于那些原本会继续吸烟的成年人、社会、公司。


7、肠-肝脏串联共培养(菲莫国际)—药物吸收和毒性过程
药物性肝脏损伤(DILI)是药物研发的主要障碍,会导致药物撤市(2021 年;2016 年)。动物模型与人体之间的差异以及日益严格的伦理要求,使得有必要采用新的药物安全性评估模型(2014 年)。这种微生理系统(MPS),也称为“芯片上的器官”,是一种通过结合微流控、微制造和三维(3D)细胞培养构建的装置。它能够为动物模型重现生理相关的器官功能。MPS平台是一种微型化的体外生理环境(Shinohara等,2021)。 这使得能够模拟和精确控制化学梯度和生物力学力,以模拟体内环境并响应。预定义的微流控通道充当工程化的血管,重现体内生理组织功能(Low 等,2020 年),并允许与其他多器官系统联合(Kulthong 等,2020 年)。此外,多器官系统能够实现实时组织功能监测(Milani 等,2022 年)。 由微流道串联的多器官芯片模型能够进一步模拟人类动态反应和内部器官相互作用(Arakawa 等,2020 年),并为药物暴露与药物效果/毒性的关系提供辅助证据。肠和肝脏是主要的吸收、分布、代谢和排泄(ADME)器官,因此在药代动力学(PK)研究中非常重要(Vernetti 等,2017 年)。
为了弥补动物模型的局限性,提出了新的药物安全性评估模型,以完善和减少现有的模型。为了在体外肠-肝脏的微生理系统(MPS)中模拟药物的吸收和代谢,并预测药代动力学和毒性效应,中国食品药品检定研究院安全评价研究所(国家药物安全评价监测中心),中国医学科学院 & 北京协和医学院,德国TissUse GmbH公司的科学家一起合作,建立了一个肠-肝脏串联培养芯片,检测了APAP(对乙酰氨基酚)过量后的急性肝脏损伤过程,并于2024年9月发表于《Food and Chemical Toxicology》杂志。
使用 Caco-2 和 HT29-MTX-E12 细胞系建立了肠类器官,同时利用 HepG2、HUVEC-T1 和经 PMA 诱导的 THP-1 以及人类肝脏星状细胞建立了肝脏类器官。使用高效液相色谱法测定 APAP 浓度,并使用 Phoenix 软件通过非房室分析法拟合药代动力学参数。肝脏损伤生物标志物天冬氨酸转氨酶和丙氨酸转氨酶的变化,以及肝脏功能标志物白蛋白表明,这两个器官芯片模型在 4 天内的短期培养是稳定的。在给药对乙酰氨基酚(APAP)后,活性氧信号增强,同时线粒体膜电位降低,caspase-3(半胱氨酸天冬氨酸蛋白酶-3)被激活,p53 信号增强,表明 APAP 过量引发了毒性反应。在肠肝脏多器官系统模型中,我们拟合了毒代动力学参数,并模拟了 APAP 过量后的肝脏毒性过程,这将有助于器官芯片在药物毒性检测中的应用。


类器官串联培养系统---HUMIMIC的参考文献
2024, Food and Chemical Toxicology, Vol. 193, Hepatotoxic assessment in a microphysiological system: Simulation of the drug absorption and toxic process after an overdosed acetaminophen on intestinal-liver-on-chip Yu Y, Sun B, Ye X, Wang Y, Zhao M, Song J, Geng X, Marx U, Li B, Zhou X
2024, Scientific reports, Vol. 14, Integrating tumor and healthy epithelium in a micro-physiology multi-compartment approach to study renal cell carcinoma pathophysiology Somova M, Simm S, Padmyastuti A, Ehrhardt J, Schoon J, Wolff I, Burchardt M, Roennau C, Caetano Pinto P
2023, Journal of Applied Toxicology, Early View, Application of a skin and liver Chip2 microphysiological model to investigate the route-dependent toxicokinetics and toxicodynamics of consumer-relevant doses of genistein
Tao TP, Brandmair K, Gerlach S, Przibilla J, Schepky A, Marx U, Hewitt NJ, Maschmeyer I, Kühnl J
2023, Journal of Applied Toxicology, Early View, Suitability of different reconstructed human skin models in the skin and liver Chip2 microphysiological model to investigate the kinetics and first-pass skin metabolism of the hair dye, 4-amino-2-hydroxytoluene
Brandmair K, Tao TP, Gerlach S, Przibilla J, Schepky A, Marx U, Hewitt NJ, Kühnl J, Maschmeyer I
2023, Scientific reports, Vol. 13, Microfluidic-based prostate cancer model for investigating the secretion of prostate-specific antigen and microRNAs in vitro
Padmyastuti A, Sarmiento MG, Dib M, Ehrhardt J, Schoon J, Somova M, Burchardt M, Roennau, Pinto PC
2023, bioRxiv, Preprint, Diseased human pancreas and liver microphysiological system for preclinical diabetes research
Rigal S, Casas B, Kanebratt KP, Wennberg Huldt C, Magnusson LU, Mullers E, Karlsson F, Clausen M, Hansson SF, Jansson Lofmark R, Ammala C, Marx U, Gennemark P, Cedersund G, Andersson TB, Vilen LK
2023, Alternatives to Laboratory Animals, OnlineFirst, Advances in Animal Models and Cutting-Edge Research in Alternatives: Proceedings of the Third International Conference on 3Rs Research and Progress, Vishakhapatnam, 2022
Naik NN, Vadloori B, Poosala S, Srivastava P, Coecke S, Smith A, Akhtar A, Roper C, Radhakrishnan S, Bhyravbhatla B, Damle M, Pulla VK, Hackethal J, Horland R, Li AP, Pati F, Singh MS, Occhetta P, Bisht R, Dandekar P, Bhagavatula K, Pajkrt D, Johnson M, Weber T, Huang J, Hysenaj L, Mallar B, Ramray B, Dixit S, Joshi S, Kulkarni M
2023, Frontiers in Pharmacology, Vol. 14, Development of a microphysiological skin-liver-thyroid Chip3 model and its application to evaluate the effects on thyroid hormones of topically applied cosmetic ingredients under consumer-relevant conditions
Tao TP, Maschmeyer I, LeCluyse EL, Rogers E, Brandmair K, Gerlach S, Przibilla J, Kern F, Genies C, Jacques C, Najjar A, Schepky A, Marx U, Kühnl J, Hewitt NJ
2022, Biomaterials and Biosystems , Vol. 7, Setup of human liver-chips integrating 3D models, microwells and a standardized microfluidic platform as proof-of-concept study to support drug evaluation
Cox B, Barton P, Class R, Coxhead H, Delatour C, Gillent E, Henshall J, Isin EM, King L, Valentin JP
2022, Journal of Extracellular Vesicles, Vol. 11, A human kidney and liver organoid-based multi-organ-on-a-chip model to study the therapeutic effects and biodistribution of mesenchymal stromal cell-derived extracellular vesicles
Nguyen VVT, Ye S, Gkouzioti V, van Wolferen ME, Yengej FY, Melkert D, Siti S, de Jong B, Besseling PJ, Spee B, van der Laan LJW, Horland R, Verhaar MC, van Balkom BWM
2022, Cells, Vol. 11, A Human Stem Cell-Derived Brain-Liver Chip for Assessing Blood-Brain-Barrier Permeation of Pharmaceutical Drugs
Koenig L, Ramme AP, Faust D, Mayer M, Flötke T, Gerhartl A, Brachner A, Neuhaus W, Appelt-Menzel A, Metzger M, Marx U, Dehne EM
2022, Pharmaceutics, Vol. 14, Proof-of-Concept Organ-on-Chip Study: Topical Cinnamaldehyde Exposure of Reconstructed Human Skin with Integrated Neopapillae Cultured under Dynamic Flow
Vahav I, Thon M, van den Broek LJ, Spiekstra SW, Ataҫ B, Lindner G, Schimek K, Marx U, Gibbs S
2022, ALTEX, A microfluidic thyroid-liver platform to assess chemical safety in humans
Kühnlenz J, Karwelat D, Steger-Hartmann T, Raschke M, Bauer S, Vural Ö, Marx U, Tinwell H, Bars R
2022, Frontiers in Toxicology, A Multi-Organ-on-Chip Approach to Investigate How Oral Exposure to Metals Can Cause Systemic Toxicity Leading to Langerhans Cell Activation in Skin
Koning JJ, Rodrigues Neves CT, Schimek K, Thon M, Spiekstra SW, Waaijman T, de Gruijl TD, Gibbs S
2021, Drug Testing and Analysis, Early view, Organ-on-a-chip: Determine feasibility of a human liver microphysiological model to assess long-term steroid metabolites in sports drug testing
Görgens C, Ramme AP, Guddat S, Schrader Y, Winter A, Dehne EM, Horland R, Thevis M
2021, Science, Vol. 373, Human microphysiological systems for drug development
Roth A, MPS-WS Berlin 2019
2021, Frontiers in Medicine, Vol. 8, An Individual Patient's "Body" on Chips – How Organismoid Theory Can Translate Into Your Personal Precision Therapy Approach
Marx U, Accastelli E, David R, Erfurth H, Koenig L, Lauster R, Ramme AP, Reinke P, Volk HD, Winter A, Dehne EM
2021, Stem Cell Research, Vol. 53, Generation of two additional integration-free iPSC lines from related human donors
Ramme AP, Faust D, Koenig L, Nguyen N, Marx U
Cell line repository/bank: Human Pluripotent Stem Cell Registry (hPSCreg)
2021, Journal of Applied Toxicology, Early view, Demonstration of the first‐pass metabolism in the skin of the hair dye, 4‐amino‐2‐hydroxytoluene, using the Chip2 skin–liver microphysiological model
Tao TP, Brandmair K, Gerlach S, Przibilla J, Géniès C, Jacques‐Jamin C, Schepky A, Marx U, J. Hewitt N, Maschmeyer I, Kühnl J
2021, Toxicology, Vol. 448, Characterization of application scenario-dependent pharmacokinetics and pharmacodynamic properties of permethrin and hyperforin in a dynamic skin and liver multi-organ-chip model
Kühnl J, Tao TP, Brandmair K, Gerlach S, Rings T, Müller-Vieira U, Przibilla J, Genies C, Jaques-Jamin C, Schepky A, Marx U, J. Hewitt N, Maschmeyer I
2020, TissUse White Paper, Multi-Organ Microphysiological Systems are Poised for Expansive Integration
2020, Scientific reports. Vol. 10, Repeated dose multi-drug testing using a microfluidic chip-based coculture of human liver and kidney proximal tubules equivalents
Lin N, Zhou X, Geng X, Drewell C, Hübner J, Li Z, Zhang Y, Xue M, Marx U, Li B
2020, In Vitro Cellular & Developmental Biology – Animal, The microfollicle: a model of the human hair follicle for in vitro studies
Ataç B, Kiss FM, Lam T, Fauler B, Edler C, Hu P, Tao TP, Jädicke M, Rütschle I, Azar RP, Youngquist S, Mielke T, Marx U, Lauster R, Lindner G, DiColandrea T
2020, International Journal of Pharmaceutics, Vol. 589, Toxicity of topically applied drugs beyond skin irritation: Static skin model vs. Two organs-on-a-chip
Tavares RSN, Tao TP, Maschmeyer I, Maria-Engler SS, Schäfer-Korting M, Winter A, Zoschke C, Lauster R, Marx U, Gaspar LR
2020, Advanced Science, Metal‐Specific Biomaterial Accumulation in Human Peri‐Implant Bone and Bone Marrow
Schoon J, Hesse B, Rakow A, Ort MJ, Lagrange A, Jacobi D, Winter A, Huesker K, Reinke S, Cotte M,Tucoulou R, Marx U, Perka C, Duda GN, Geissler S
2020, Human Reproduction, Vol. 35, A multi-organ-chip co-culture of liver and testis equivalents: a first step toward a systemic male reprotoxicity model
Baert Y, Ruetschle I, Cools W, Oehme A, Lorenz A, Marx U, Goossens E, Maschmeyer I
2020, Scientific Reports, Human multi-organ chip co-culture of bronchial lung culture and liver spheroids for substance exposure studies
Schimek K, Frentzel S, Luettich K, Bovard D, Rütschle I, Boden L, Rambo F, Erfurth H, Dehne EM, Winter A, Marx U, Hoeng J
2020, Journal of Tissue Engineering and Regenerative Medicine, Vol. 14, Reconstructed human skin shows epidermal invagination towards integrated neopapillae indicating early hair follicle formation in vitro
Vahav I, van den Broek LJ, Thon M, Monsuur HN, Spiekstra SW, Atac B, Scheper RJ, Lauster R, Lindner G, Marx U, Gibbs S
2020, ALTEX, Preprint, Biology-inspired Microphysiological systems to advance patient benefit and animal welfare in drug development
Marx U, Akabane T, Andersson T, Baker E, Beilmann M, Beken S, Brendler-Schwaab S, Cirit M, David R, Dehne EM, Durieux I, Ewart L, Fitzpatrick S, Frey O, Fuchs F, Griffith L, Hamilton G, Hartung T, Hoeng J, Hogberg H, Hughes D, Ingber D, Iskandar A, Kanamori T, Kojima H, Kuehnl J, Leist M, Li B, Loskill P, Mendrick D, Neumann T, Pallocca G, Rusyn I, Smirnova L, Steger-Hartmann T, Tagle D, Tonevitsky A, Tsyb S, Trapecar M, van de Water B, van den Eijnden-van Raaij J, Vulto P, Watanabe K, Wolf A, Zhou X, Roth A
2020, Current Opinion in Toxicology, Journal pre-proof, The universal physiological template – a system to advance medicines
Dehne EM, Marx U
2020, Elsevier, 441-462, Automation and opportunities for industry scale-up of microphysiological systems in: Organ-on-a-Chip: Engineered Microenvironments for Safety and Efficacy Testing
Dehne EM, Erfurth H, Muhsmann AK, Marx U
2020, Elsevier, 429-439, Human body-on-a-chip systems in: Organ-on-a-Chip: Engineered Microenvironments for Safety and Efficacy Testing
Dehne EM, Marx U
2019, Stem Cell Research, Vol. 41, Generation of four integration-free iPSC lines from related human donors
Ramme AP, Faust D, Koenig L, Marx U
Cell line repository/bank: Human Pluripotent Stem Cell Registry (hPSCreg)
2019, Current Opinion in Toxicology, Vol. 17, Microphysiological systems in the evaluation of hematotoxicities during drug development
Dehne EM, Winter A, Marx U
2019, Future Science OA, Vol. 5, No. 8, Autologous induced pluripotent stem cell-derived four-organ-chip
Ramme AP, Koenig L, Hasenberg T, Schwenk C, Magauer C, Faust D, Lorenz AK, Krebs AC, Drewell C, Schirrmann K, Vladetic A, Lin GC, Pabinger S, Neuhaus W, Bois F, Lauster R, Marx U, Dehne EM
2019, Elsevier, 279-284, Biologically-Inspired Microphysiological Systems in: The History of Alternative Test Methods in Toxicology
Dehne EM, Hickman J & Shuler M
2018, ALTEX, Optimizing drug discovery by Investigative Toxicology: Current and future trends
Beilmann M, Boonen H, Czich A, Dear G, Hewitt P, Mow T, Newham P, Oinonen T, Pognan F, Roth A, Valentin JP, Van Goethem F, Weaver RJ, Birk B, Boyer S, Caloni F, Chen AE, Corvi R, Cronin MTD, Daneshian M, Ewart LC, Fitzgerald RE, Hamilton GA, Hartung T,Kangas JD, Kramer NI, Leist M, Marx U, Polak S, Rovida C, Testai E, Van der Water B, Vulto P, Steger-Hartmann T
2018, Nature Scientific Reports, Simultaneous evaluation of anti-EGFR-induced tumour and adverse skin effects in a microfluidic human 3D co-culture model
Hübner J, Raschke M, Rütschle I, Gräßle S, Hasenberg T, Schirrmann K, Lorenz A, Schnurre S, Lauster R, Maschmeyer I, Steger-Hartmann T, Marx U
2018, Bioengineering 2018, Bioengineering of a Full-Thickness Skin Equivalent in a 96-Well Insert Format for Substance Permeation Studies and Organ-on-a-Chip Applications
Schimek K, Hsu HH, Boehme M, Kornet JJ, Marx U, Lauster R, Pörtner R, Lindner G
2018, J Vis Exp., A Method for Determination and Simulation of Permeability and Diffusion in a 3D Tissue Model in a Membrane Insert System for Multi-well Plates
Hsu HH, Kracht JK, Harder LE, Rudnik K, Lindner G, Schimek K, Marx U, Pörtner R
2018, Stem Cell Res Ther., The role of fibrinolysis inhibition in engineered vascular networks derived from endothelial cells and adipose-derived stem cells
Mühleder S, Pill K, Schaupper M, Labuda K, Priglinger E, Hofbauer P, Charwat V, Marx U, Redl H, Holnthoner W
北京佰司特科技有限责任公司 (https://www.best-sciences.com/)
类器官串联芯片培养仪—HUMIMIC;灌流式细胞组织类器官代谢分析仪—IMOLA;光片显微镜—LSM-200;
蛋白稳定性分析仪—PSA-16;单分子质量光度计—TwoMP;超高速视频级原子力显微镜—HS-AFM;微流控扩散测量仪—Fluidity One-M;
电荷光度计—illumionONE;全自动半导体式细胞计数仪—SOL COUNT;农药残留定量检测仪—BST-100;台式原子力显微镜—ACST-AFM;微纳加工点印仪—NLP2000DPN5000;






